ChemicalEquations ChemicalReactions Chemistry
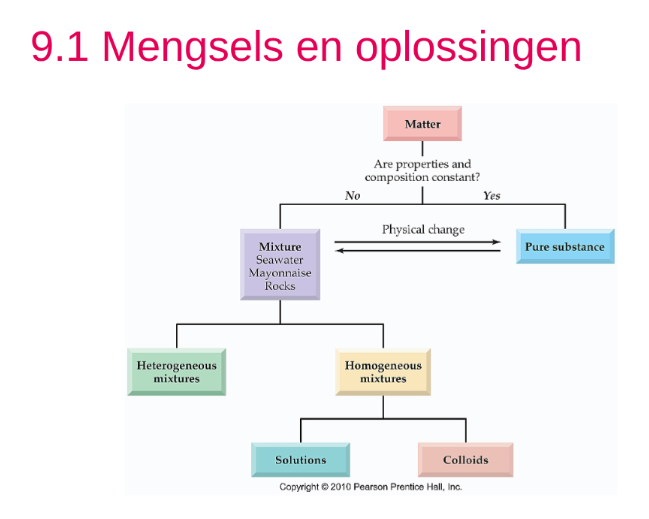
9.1 mengsels en oplossingen
Homogene Mengsels
Oplossingen en Colloiden
Op basis van grootte van deeltjes:

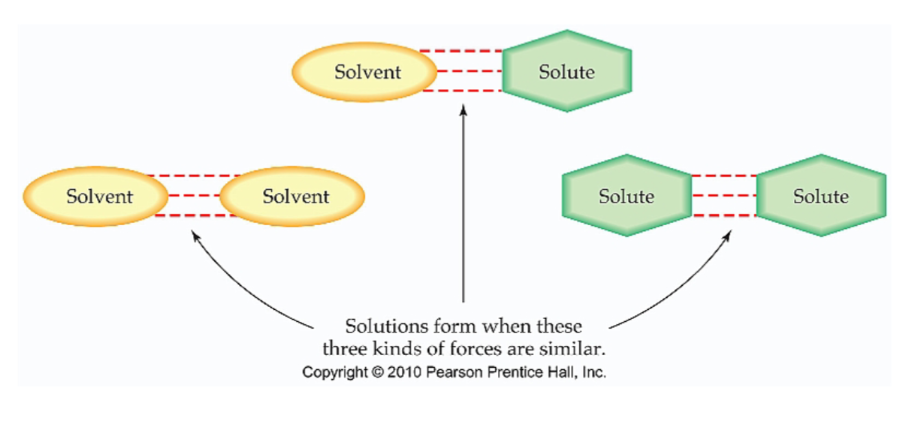
9.2 Het oplosprocess
Wanneer lost een stof op in een oplosmiddel?
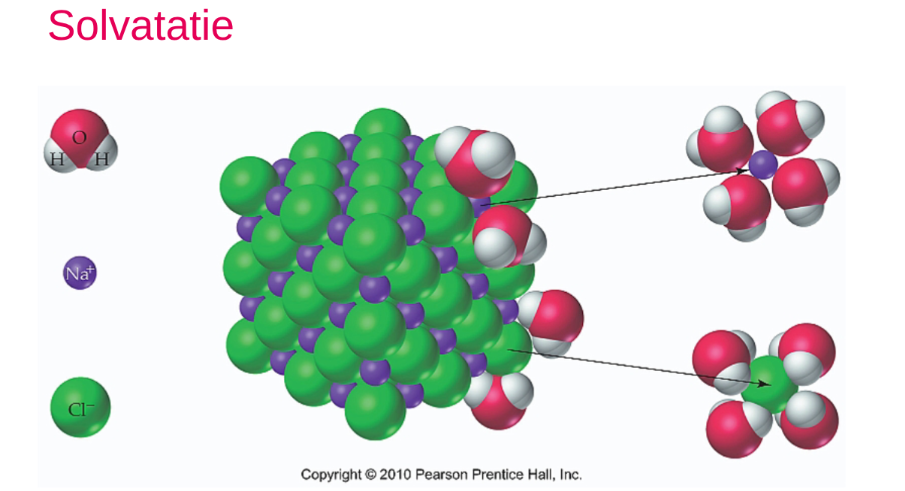
9.3 Vaste Hydraten
Sommige ionen trekken zo hard aan water dat ze watermoleculen in vaste toestand kunnen vasthouden. Hydraten
9.4 Oplosbaarheid
Mengbaar (‘miscible’)
-
oplossing vormt in alle proporties (lost altijd op)
- bijv ethanol en water
-
Verzadigd
- Oplossing die de maximale hoeveelheid opgeloste stof bevat bij equilibrium
-
Oplosbaarheid
- Maximale hoeveelheid dat een stof in een zekere hoeveelheid oplosmiddel opgelost kan worden bij een bepaalde temperatuur (g/100mL)
9.6 invloed van druk op oplosbaarheid
NIET
9.8 Verdunnen
Oplosmiddel toevoegen aan een oplossing.
- de hoeveelheid opgeloste stof verandert niet
- Het volume wordt groter
- dus de concentratie wordt kleiner Vvoor x Cvoor = Vna x Cna
9.9 Elektrolyten
Stoffen die opgelost in water en/of in gesmolten toestand, stroom geleiden.
Sterke zwakke en niet-elektrolyten
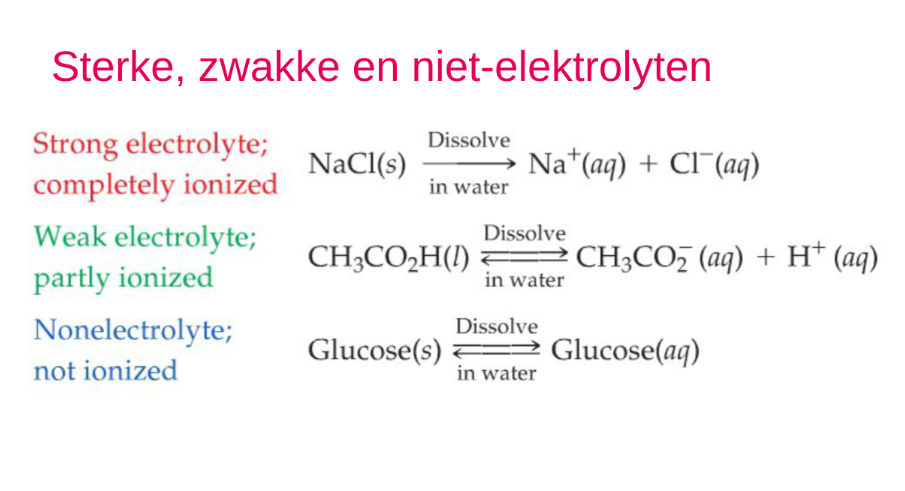
9.11 Eigenschappen van oplossingen
Colligatieve eigenschappen
- die eigenschappen die zuiver door het aantal deeltjes in het systeem en niet door hun massa bepaald worden

9.12 Osmose en osmotische druk
wat is ..?
- Diffusie
- is een proces ten gevolge van de willekeurige beweging van deeltjes
- Deze willekeurige beweging is het gevolg van de kinetische energie die de deeltjes bezitten
- Bij verschillen in concentratie leidt tot diffusie tot een netto verplaatsing van deeltjes van plaatsen met hoge concentratie naar plaatsen met een lage concentratie
- Osmose
- dit is een proces op basis van diffusie waarbij een vloeistof, waarin stoffen zijn opgelost, door een semipermeabel membraan stroomt zonder de opgeloste stoffen
- Osmotische druk
- dit is het drukverschil dat tussen twee oplossingen van verschillende concentraties ontstaat ten gevolge van osmose
- Osmolariteit
- Dit is de concentratie van osmotisch actieve stoffen in een oplossing
- Uitgedrukt in het aantal osmolen per liter
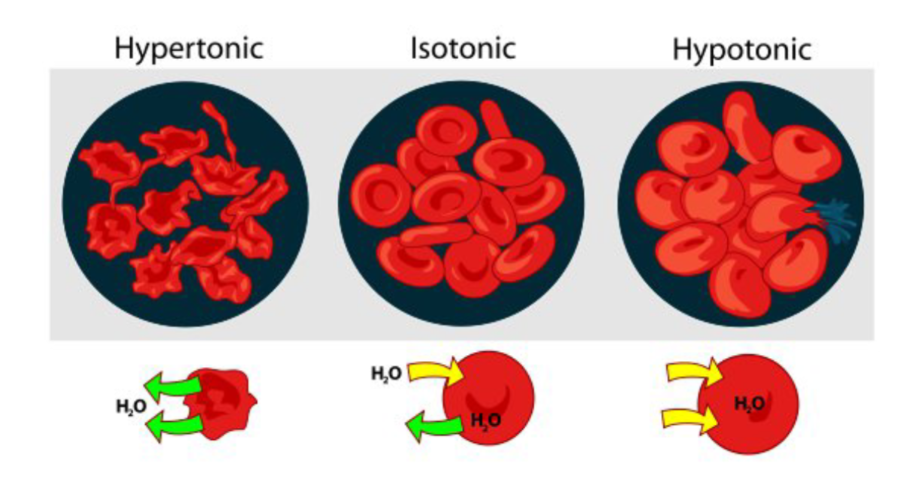
- Isotoon
- concentratie stoffen is gelijk binnen en buiten de cel
- Hypo**toon*
- Hypo betekent te weinig en betreft de situatie buiten de cel
- lagere concentratie buiten de cel > dus de cel neemt water tot zich
- Hypo betekent te weinig en betreft de situatie buiten de cel
- Hyper**toon*
- Hyper betekent te veel en betreft de situatie buiten de cel
- hogere concentratie buiten de cel > dus de cel verliest water
- Hyper betekent te veel en betreft de situatie buiten de cel