ChemicalEquations ChemicalReactions Chemistry
8.2 Intermoleculaire Krachten
Krachten tussen moleculen
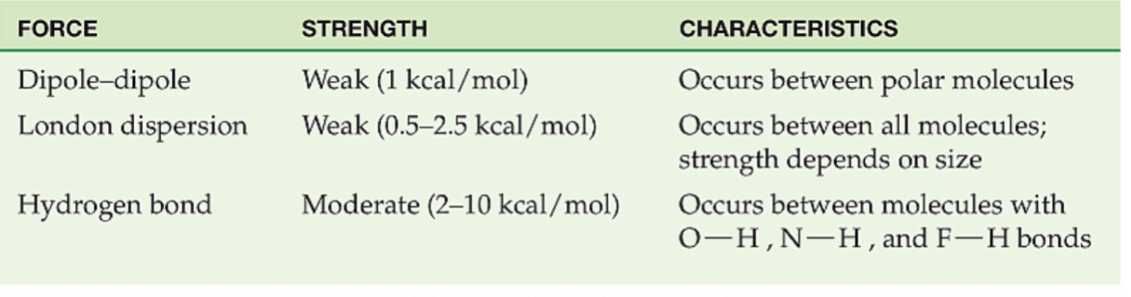
- dipool-dipool
- london dispersiekrachten
- waterstofbruggen
Dipool-dipool Interacties
een Dipool-dipoolbinding ontstaat wanneer twee polaire moleculen bij elkaar komen. De lichte verschillen in lading in de moleculen zorgen voor een lichte magneetwerking, zodat de polen in de moleculen hun tegenpolen in omringende moleculen gaan aantrekken. Hierdoor trekken de moleculen naar elkaar toe en vormen ze een soort netwerk.
Verschil in kookpunt
een dipool-dipool interactie verhoogt het kookpunt
Geinduceerde dipool
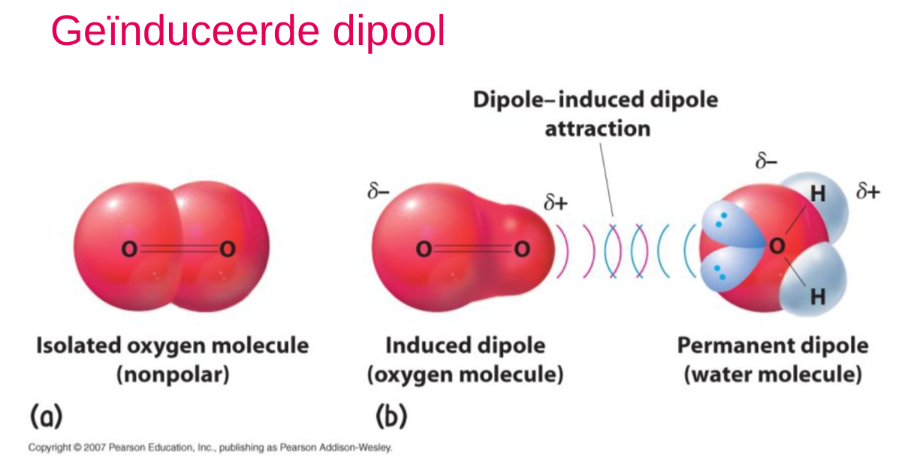
London dispersiekrachten
londonkrachten zijn zwakke intermoleculaire krachten die ontstaan uit de aantrekkende krachten tussen tijdelijke dipolen in anders apolaire moleculen.
- London krachten worden soms vanderwaalskrachten genoemd
- hoewel ze feitelijk hier een deel van uitmaken
Vanderwaalskrachten
bestaat uit:
- londondispersiekrachten
- Dipool-dipool Interacties
- Geinduceerde dipool-dipool interacties
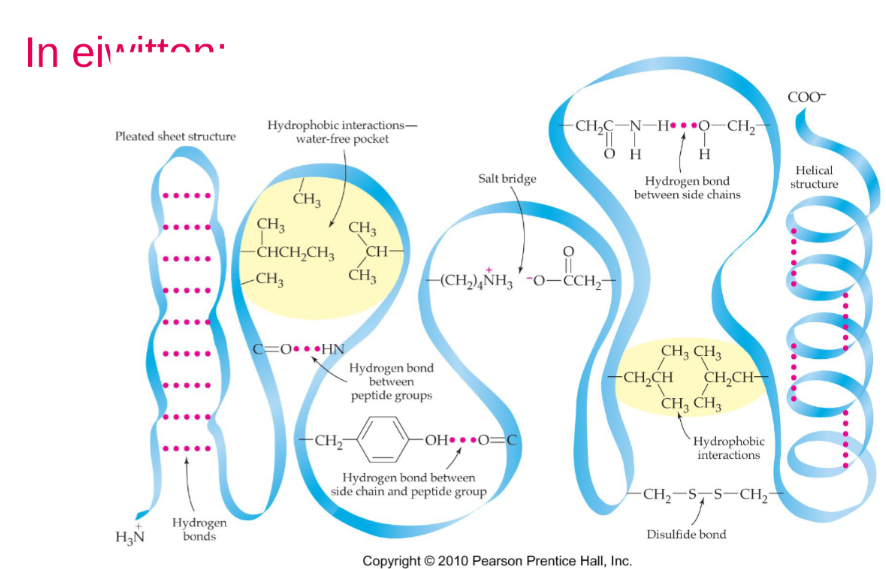
Waterstofbruggen
een waterstofbrug is een intermoleculaire kracht tussen een elektronenpaar op een sterk elektronenegatief atoom
- *zuurstof
- *stikstof
- fluor
en een naburig H-atoom gebonden aan een ander sterk elektronenegatief atoom
In eiwitten