biochem week1
Week 1 - Chemische evenwichten zwakke zuren en basen (3).pdf
Paginas 5 - 9 EN 17 - 29 page=5 page=17
Dynamisch evenwicht
heen en weer gaande reactie vinden tegelijk plaats De reactiesnelheden zijn gelijk, i.e. in evenwicht
Dit word aangeduid door het volgende teken ⇄
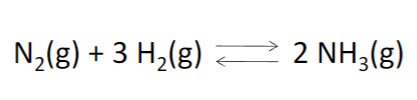
De berekening voor de Kc (het eventwicht constant) is het zelfde als Ka

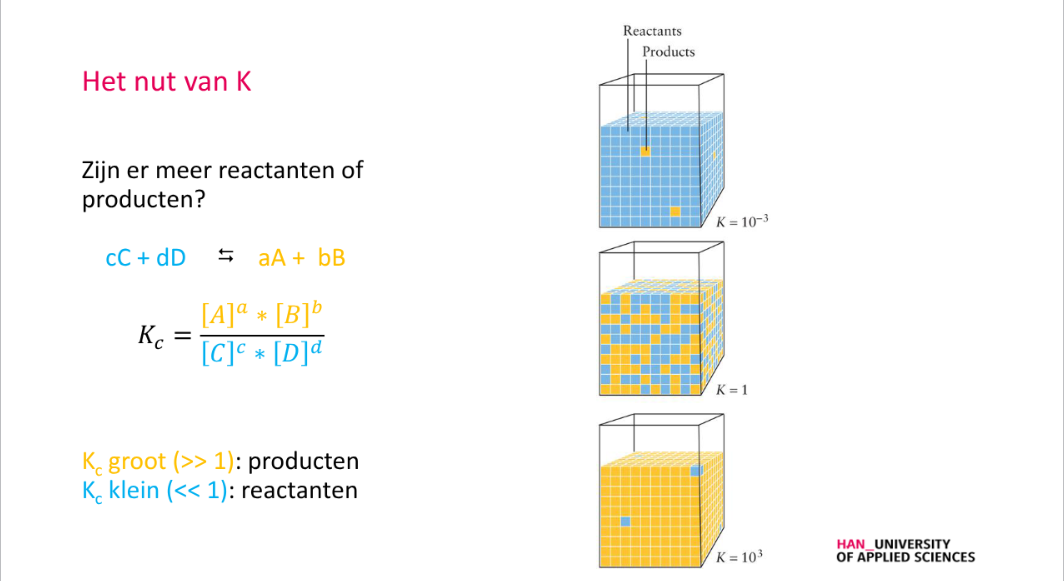


Rekenregels
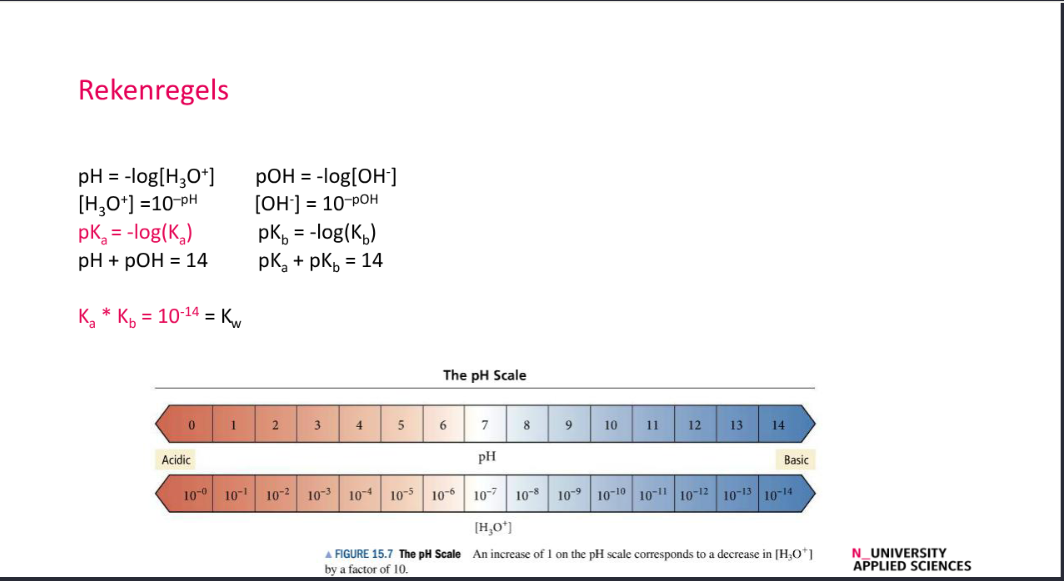
10.1
Bronsted-Lowry
Zuur = protonendonor Base = Protonenacceptor
Een proton is waterstof (H)

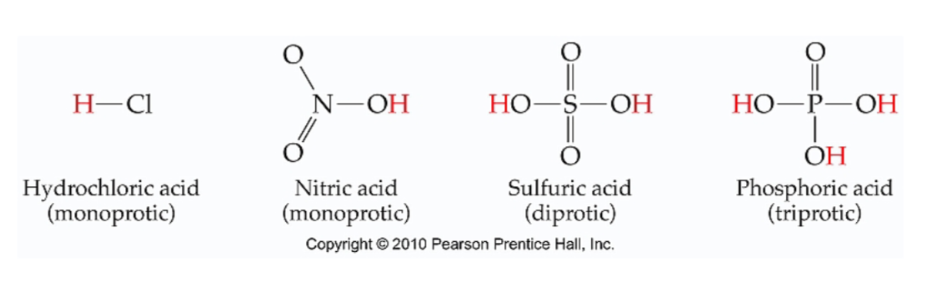
Meerwaardige zuren
Meerwaardige zuren kunnen meerdere protonen afstaan, bijv:
- H2SO4
- H2SO
- H3PO4
Zuur-base reactie
Proton overdracht
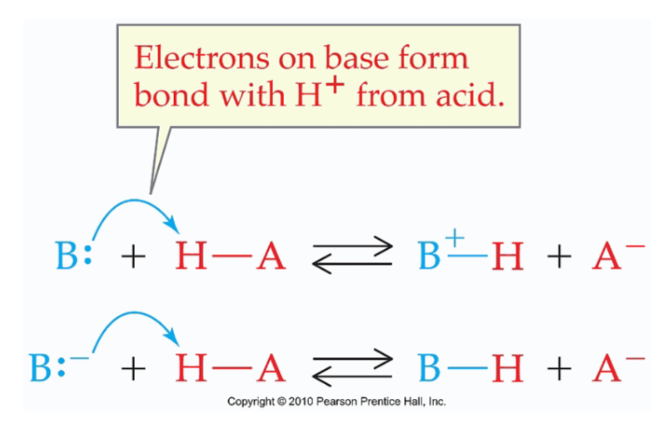
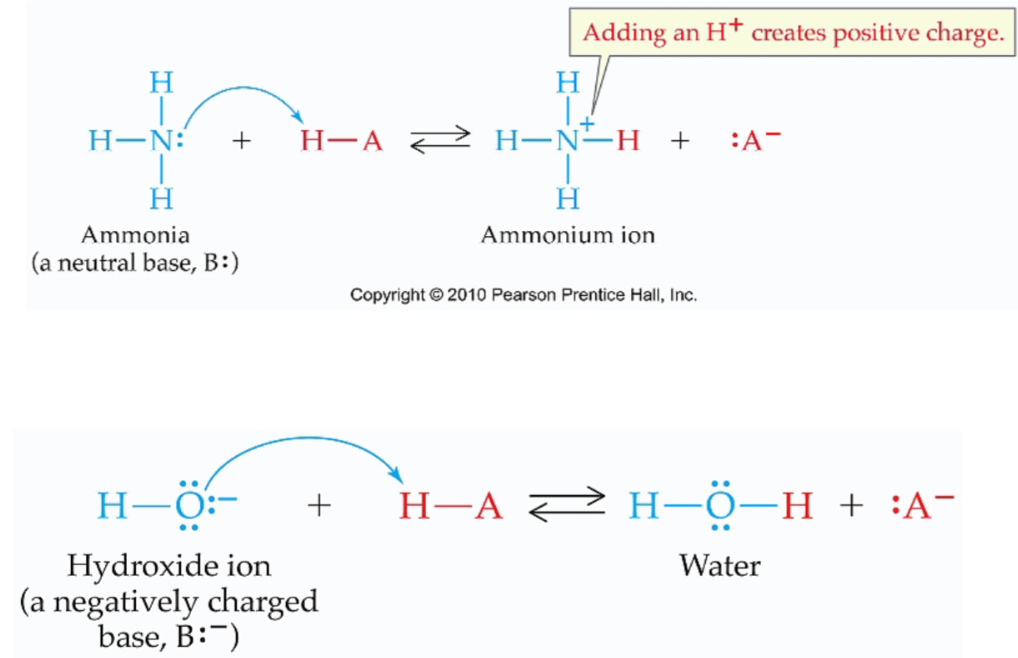
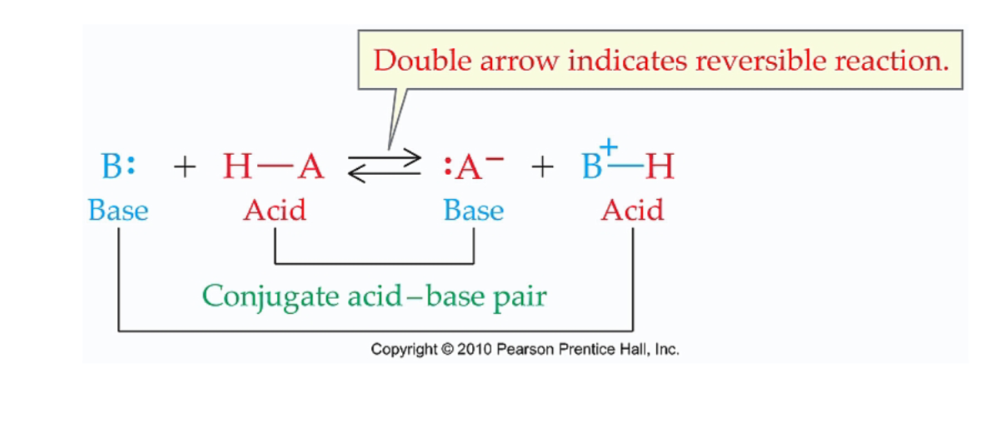
Geconjugeerd zuur-base paar
Het zuur heeft een H+ meer dan zijn Geconjugeerde base
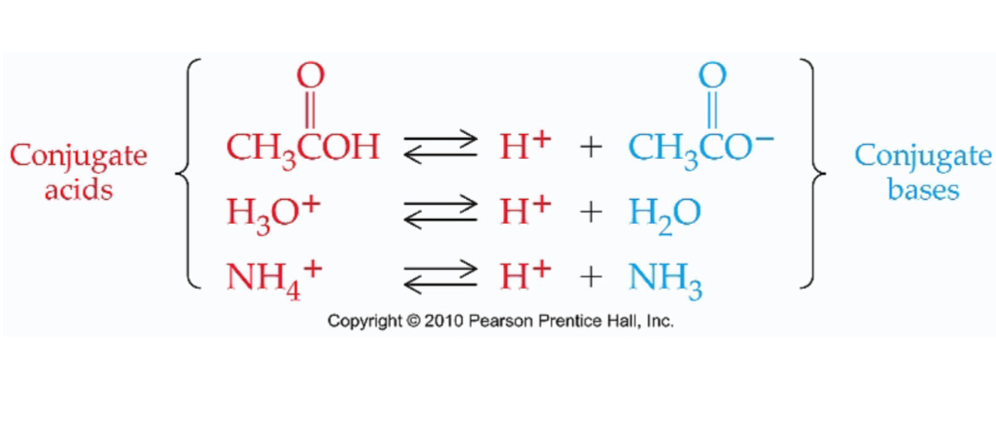
10.2 Sterke en Zwakke zuren

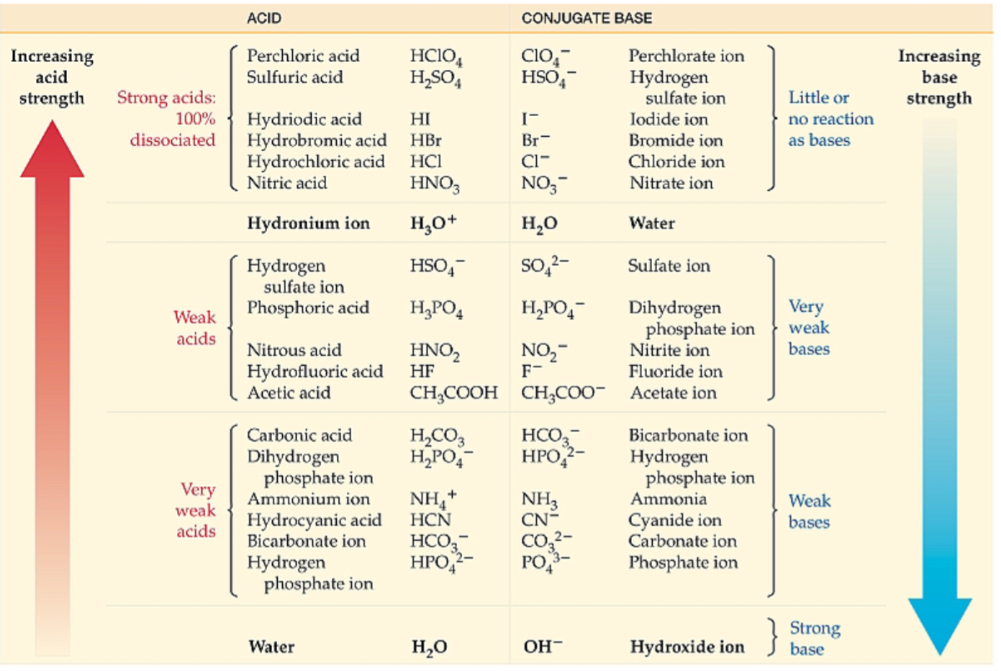
Sterke zuren
Sterke zuren hebben een Ka die veel groter is dan 1
- omdat ze geheel splitsen.

Zwakke zuren
Zwakke zuren hebben een Ka die veel kleiner is dan 1
- omdat het gedeelte moleculen dat splitst kleiner is dan het gedeelte moleculen dat niet splitst.

H10.3 Zuur (Ionisatie) constante
- Het afstaan van een proton door meerwaardige zuren gaat moeilijker naarmate er meer protonen afgesplitst zijn
- de Ka van elke volgende stap is kleiner.
- De meeste organische zuren (met COOH) hebben een Ka in de buurt van 10-5


10.4 - Water is een zuur en een base
Pagina 23 Chemie Aantekeningen BASIB.pdf
Amfolyten: Stoffen die zowel zuur als base kunnen zijn
Water als Base
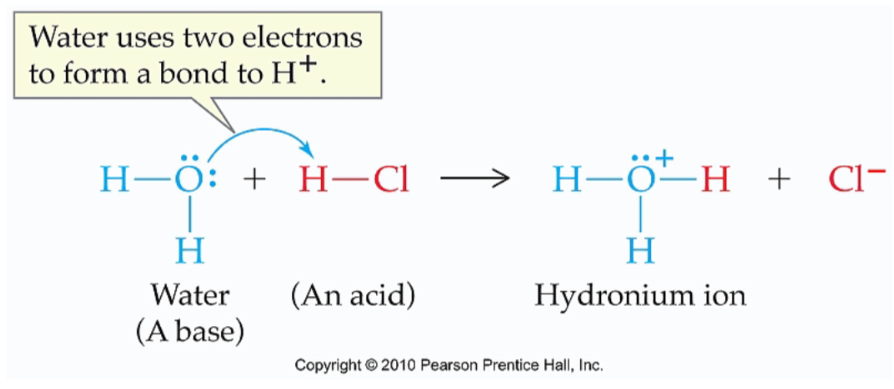
Water als zuur

10.10 Bufferoplossingen