Basis van zuren en basen
Zuur:
- Oplossing met een PH lager dan 7
- Heeft H+
Base:
- Een oplossing met een PH hoger dan 7
- Heeft OH-
Neutralisatie:
- Door een zuur en base te mengen krijg je water en zout.
- zout bestaat uit kation van de base en anion van het zuur
Brønsted-Lowry
Brønsted en Lowry waren 2 onderzoekers.
Een zuur is een protondonor.
Een base is een protonenacceptor.
Een proton = H+
Meerwaardige zuren kunnen meerdere protonen afstaan, bijvoorbeeld:
- H2SO4
- H2S
- H3PO4
Een zurige H valt sneller af dan een niet-zurige H.
Geconjugeerde zuur-base paren
Het zuur heeft een H+ meer dan z’n geconjugeerde base.
Geconjugeerde zuur-base paar:
- Een zuur-base paar die beide kanten op kan, de base wordt zuur en zuur wordt base. Dit is dus een evenwichtsreactie.
Sterke en zwakke zuren
Sterke zuren en basen splitsen volledig in ionen.
Zwakke zuren en basen splitsen gedeeltelijk in ionen.
Dus:
- Sterk = Volledige splitsing.
- Zwak = Gedeeltelijke splitsing.
De sterkere oplossing trekt harder en daar zal je meer van krijgen, het evenwicht zal daarnaar toe leunen.

Zuurconstante (Ka): De constante van het evenwicht waarin een zuur wordt opgelost in water.
Sterke zuren hebben een Ka die veel groter is dan 1 omdat ze geheel splitsen.
Zwakke zuren hebben een Ka die veel kleiner is dan 1 omdat het gedeelte moleculen dat splitst kleiner is dan het gedeelte moleculen dat niet splitst.

Water als zuur en base
Water is zowel een zuur als base
Water als een base:
 Water als een zuur:
Water als een zuur:

Amfolyt: Kan zowel een H+ opnemen als afstaan.
Autoprotolyse: Een stof reageert met zichzelf. Dus: Autoprotolyse van water → Water reageert met zichzelf.
Meten van pH in een waterige oplossing
pH is een maat voor de zuurgraad van een oplossing
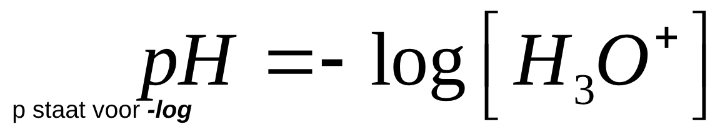
Bufferoplossingen
- Combinatie van stoffen die drastische veranderingen in de pH voorkomen.
- Een zwak zuur en z’n geconjugeerde base zitten samen in één oplossing!
Bufferoplossing:
- Oplossing waar zowel een zuur als een base in zit.
- Het pH schommelt niet te veel ook al worden er stoffen aan toe gevoegd.
Bijvoorbeeld:
- Bloed
Je moet de pH van een bufferoplossing kunnen berekenen, de formule daarvoor is: pH = pKa + log (geconjugeerde base)/(zuur) of: pH = pKa - log ((zuur)/(geconjugeerde base))
-log(Ka) = -pKa
Als er een zout staat, mag je die vaak herschrijven. (zie dia 26 voor voorbeeld-berekening)